Mögliche Hilfe für Hunderttausende Patienten mit Herzschwäche
Einen neuartigen Früherkennungsmarker, der über solche Diagnose- und Prognose-Qualitäten verfügen könnte, haben der Privatdozent Dr. med. Benjamin Meder und Kollegen an der Klinik für Kardiologie des Universitätsklinikums Heidelberg (Direktor: Prof. Dr. med. Hugo A. Katus), dem Zentrum für Bioinformatik der Universität Saarland (Prof. Dr. rer. nat. Andreas Keller) und einem Unternehmen mit Expertise in der Molekulardiagnostik identifiziert. Die Forschungsarbeit „Epigenome-wide Association Study Identifies Cardiac Gene Patterning and A Novel Class of Biomarkers for Heart Failure“ erscheint im renommierten Fachjournal Circulation (DOI: 10.1161/CIRCULATIONAHA.117.027355).
Das Team um Dr. Meder konnte erstmals zeigen, dass epigenetische DNA-Methylmarkierungen und ihre steuernde Funktion für die Genaktivität sehr gute Biomarker-Qualitäten für die Diagnose der Herzinsuffizienz aufweisen. „Neuartige Früherkennungsmarker auf Basis der Erkenntnisse von PD Meder könnten enorm zu einer besseren Diagnose und zielgenauen Therapie der Herzschwäche der meist älteren Patienten über 65 Jahre verhelfen. Außerdem erfordert dieser Ansatz nur eine einfache Blutanalyse und keine Herzbiopsie“, würdigt Prof. Dr. med. Thomas Voigtländer, Vorstandsmitglied der Deutschen Herzstiftung, die Forschungsleistung des Heidelberger Forschers. Aufgrund des für die Herz-Diagnostik enormen Potenzials dieser Erkenntnisse wurde diese Forschungsarbeit mit dem Wilhelm P. Winterstein-Preis 2017 der Deutschen Herzstiftung (Dotation: 10.000 Euro) ausgezeichnet. Allein 2015 wurden in Deutschland rund 445.000 Patienten mit einer Herzschwäche in ein Krankenhaus eingeliefert; über 44.500 starben 2014 daran.
Veränderungen des Epigenoms im Herzen und Blut bei Herzschwächepatienten nachgewiesen
Epigenetische Faktoren steuern durch DNA-Methylierung die Aktivität von Genen und bilden darin eine Art Bindeglied zwischen der genetischen Information im Erbgut des Menschen, seiner zellulären Genprogramme und seiner Umwelt. Die Gesamtheit der epigenetischen Faktoren wird als Epigenom bezeichnet. Bei der DNA-Methylierung werden Methylgruppen, kleine Moleküle, nur an eine ganz spezielle Kombination von DNA-Bausteinen übertragen, was insbesondere in Cytosin-Guanin-Dinukleotiden (CpG) erfolgt. Dr. Meder und Kollegen konnten in ihrer Studie erstmals den Zusammenhang zwischen DNA-Basencode, DNA-Methylierung und Aktivität der Genprogramme bei Herzschwäche nachweisen. Untersucht hat Dr. Meder die Epigenom-weite DNA-Methylierung (ca. 500.000 CpG-Dinukleotide) sowohl in Herzgewebeproben als auch im Blut von Patienten mit Herzschwäche. Durch parallele DNA- und RNA-Sequenzierung wurde die Aktivität des gesamten Genprogramms des Herzens bestimmt und eine „Landkarte“ der Epigenetik der Herzschwäche erstellt.
Robuste Früherkennungsmarker für Herzschwäche
Als kritische epigenetische Regionen wurden insgesamt 517 CpGs identifiziert, die eng mit einer Herzschwäche und der Genregulation in Verbindung stehen. Unter diesen befinden sich auch Marker, die sich für die frühe Diagnose der Herzschwäche eignen. „B9 Protein Domain 1, kurz B9D1 zum Beispiel ist ein Gen, das bei der Herzentwicklung eine wichtige Rolle innehat. Der Methylierungs-Status von B9D1 eignet sich aber auch für die frühe Diagnose der Herzschwäche. Darin scheint dieser Marker in seiner Aussagekraft auch NT-proBNP als Gold-Standard-Marker überlegen“, bestätigt PD Meder. Allerdings müssten weitere Studien die Bedeutung von DNA-Methylierungsmarkern wie B9D1 für die klinische Routineanwendung klären, um vorschnelle Rückschlüsse auf eine mögliche Überlegenheit dieser neuartigen Marker gegenüber bestehenden Biomarkern zu vermeiden.
Der Wilhelm P. Winterstein-Preis wird alljährlich für eine wissenschaftlich herausragende Arbeit auf dem Gebiet der Herz-Kreislauf-Erkrankungen, bevorzugt aus einem patientennahen Forschungsbereich, vergeben.
Die Forschungsarbeit von PD Meder wird vom Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK) gefördert.
[Infokasten]
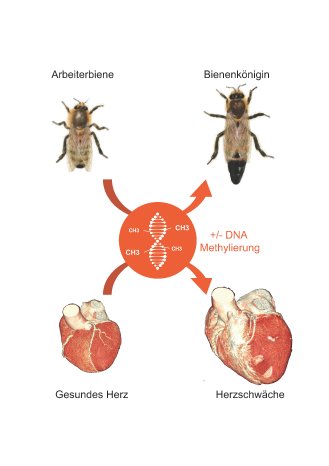
Die Bedeutung der Epigenetik für Entwicklungsprozesse in der Tierwelt und in der Herzmedizin am Beispiel der Bienenlarve und der Herzschwäche
Das Wort Epigenetik ist vom griechischen epigenesis abgeleitet und bedeutet sinngemäß „nachträgliche Entstehung“. Anhand der Bienenlarve lässt sich dies eindrucksvoll verdeutlichen: Genetisch – d. h. in der Abfolge der DNA-Basen des Erbguts – sind die Arbeiterbiene und die Bienenkönigin nahezu identisch. Durch einen Umweltfaktor, und zwar durch verlängerte Fütterung mit Gelée Royal, werden bestimmte Enzyme gehemmt und dadurch weniger Methylierungsgruppen (-CH3) an die DNA angefügt. Hierdurch werden die zugehörigen Genabschnitte aktiviert. Alleine durch diesen Prozess kommt es zu einer erstaunlichen Gestaltwandelung und somit zur Programmierung des Lebenszyklus der Biene: Die genetisch identische Larve wird durch DNA-Methylierung (-CH3) zur Arbeiterbiene bzw. durch Hemmung der Methylierung zur Bienenkönigin.
Ob ähnliche Veränderungen der DNA-Methylierung wie bei den Bienen auch bei humanen Herzerkrankungen auftreten, diese Frage hat sich PD Meder gestellt. Denn für bestimmte Erkrankungen wie Krebs spielen dieselben Mechanismen eine bedeutende Rolle. Durch den Einsatz modernster Technologien konnten er und sein Team weltweit zum ersten Mal DNA-Methylierung, DNA-Basencode und RNA-Entstehung in Blut und Herzgewebe von Patienten mit Herzschwäche untersuchen. „Die Ergebnisse eröffnen eine komplett neuartige Sichtweise auf ein bisher bei Herzerkrankungen kaum erforschtes Gebiet“, so PD Meder.